
| 病例1 | |
 | 品种:短毛猫 |
| 年龄:13岁 | |
| 性别:雄 | |
| 是否绝育:是 | |
| 诊断:肝外胆道梗阻 | |
01 主诉及病史
进一步评估继发于胆管癌的胆道梗阻。
CT扫描和剖腹探查术发现了一个不可切除的肿块,涉及整个胆总管并延伸至肝门,存在进行性弥漫性肝内胆管扩张。肿块活检符合胆管癌。
既往治疗包括放置食管造口管,单剂量180 mg/m2 IV卡铂,住院接受静脉输液、氨苄青霉素/舒巴坦、维生素B复合物、维生素K1、马罗吡坦、赛庚啶、泮托拉唑和加巴喷丁。先前服用过罗贝考昔、米氮平、加巴喷丁和含有水飞蓟素、N-乙酰半胱氨酸、锌和维生素E的补充剂。
02 检查
体重4.65公斤。剖腹探查术后8日,肝酶活性和胆红素显著升高,中性粒细胞增多左移、对称性二甲基精氨酸升高,低钾血症和低白蛋白血症。
腹部超声发现肝脏高回声伴肝内导管扩张,无临床相关胆囊扩张,远端胆总管有低回声结节(约0.6 cm)。双侧慢性肾病和少量腹腔积液。
建议行剖腹探查及胆道支架置入术。
03 治疗
接受维生素K1(0.5 mg/kg SC,q12h)和脱氨基-D-精氨酸加压素(DDAVP,术前15分钟1.0 u/kg SC)预处理,以尽量减少出血风险。
剖腹探查证实继发于肿瘤的胆道梗阻。使用18-Ga IV导管进行胆囊穿刺,试图获得胆道通路,因为整个胆总管都充满了肿瘤,且肿瘤阻塞了胆囊管,因此没有成功。
然后使用22-Ga IV导管在术中超声引导下穿刺左外侧叶扩张的肝内胆管,成功获得胆道通路。顺行胆管造影证实肝内导管在肝门水平和整个胆总管存在阻塞(下图A)。
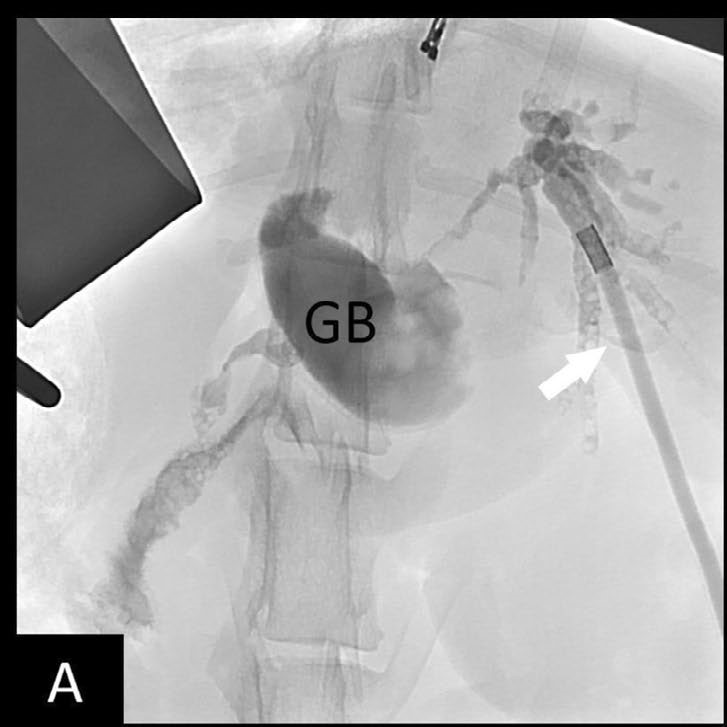
↑(A)透视显示导管(白色箭头)在肝内导管内,并成功进行了胆管造影。胆囊,GB。
一根0.018英寸的亲水导丝穿过导管并进入肝内胆道系统。将22 Ga导管更换为4 Fr微穿刺系统,导丝更换为0.035英寸加硬角尖亲水导丝。在透视引导下,导丝穿过肿瘤和胆总管(下图B)并进入十二指肠。
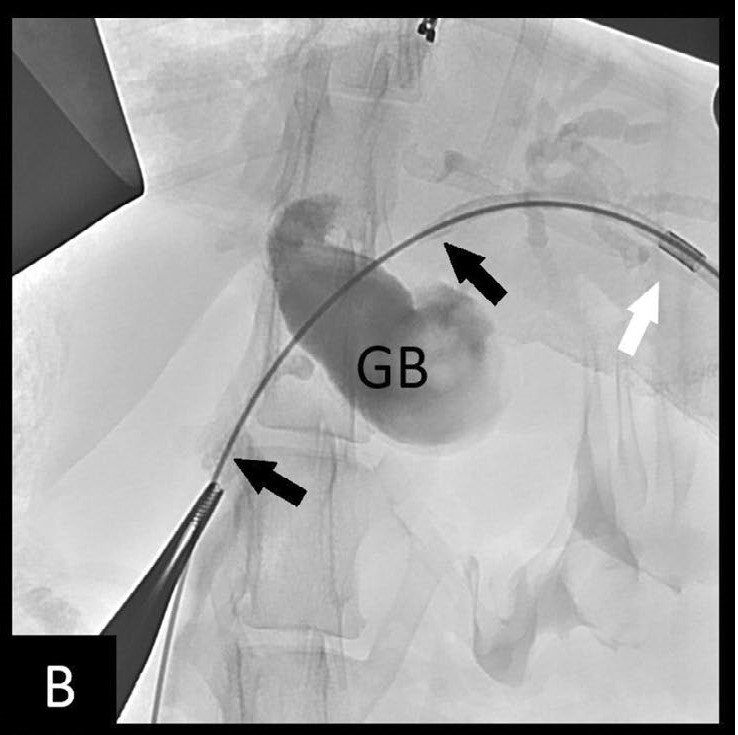
↑(B)亲水导丝(黑色箭头)穿过胆总管并进入十二指肠。
在降十二指肠上做一个小孔,以获得贯穿导丝的通道。然后将6×60 mm非覆盖自膨胀金属支架逆行推进到导丝上,从十二指肠向上并进入左肝内胆管(下图C)。
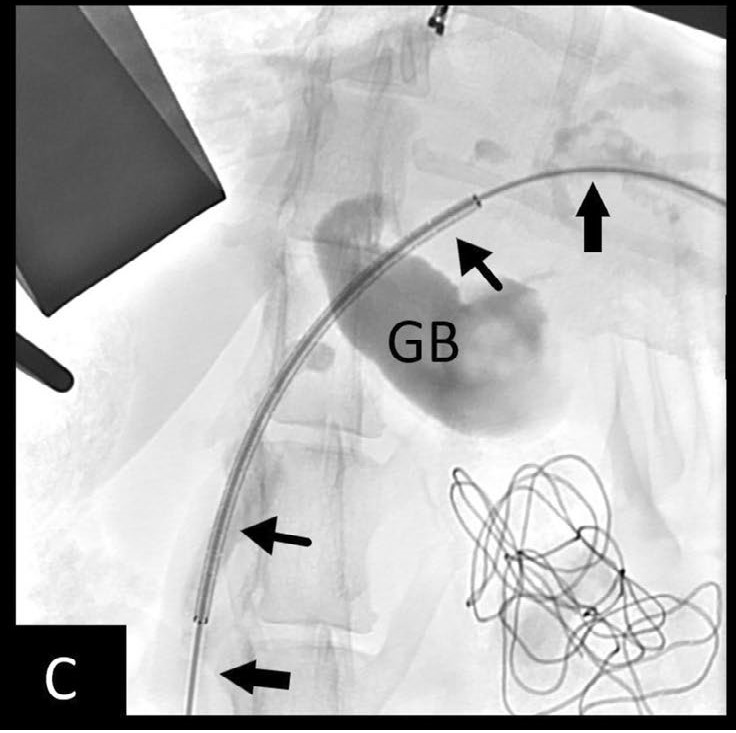
↑(C)胆道支架输送系统(黑色箭头)通过导线。
支架穿过胆总管并进入十二指肠(下图D),从而对肝脏的左侧进行减压。将锁环导管从肝侧通过导丝送入,并盘绕到左胆管中,用于未来潜在的化疗。导管的远端使用钝性解剖穿过体壁并连接到皮下通路端口以备将来通路。
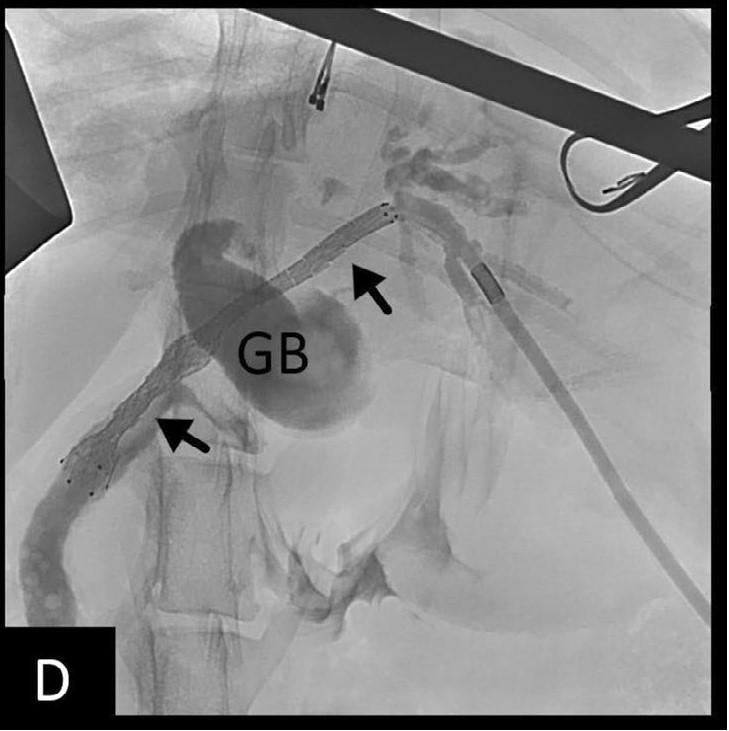
↑(D)胆管造影显示已展开的胆道支架(黑色箭头)的通畅性,引流管最终被放置在肝内导管内。
总手术时间为97分钟。胆道穿刺时采集的胆汁进行需氧和厌氧培养,所有培养均为阴性。
04 预后
住院3天,接受静脉输液、氨苄青霉素/舒巴坦(30 mg/kg IV q8h)、恩诺沙星(5 mg/kg IV q24h)、维生素 K1(0.5 mg/kg SC q12h)、昂丹司琼(0.5 mg/kg IV q12h)、泮托拉唑(1 mg/kg IV q12h)、熊去氧胆酸(13.5 mg/kg,饲管,q24h)、美沙酮(0.2 mg/kg IV q6h)、维生素B复合物和甲氧氯普胺(2 mg/kg/天 IV)。
术后1天,高胆红素血症改善,肝细胞酶活性最初增加,随后逐渐降低。术后X光片确认支架和胆道引流导管的正确放置(下图)。
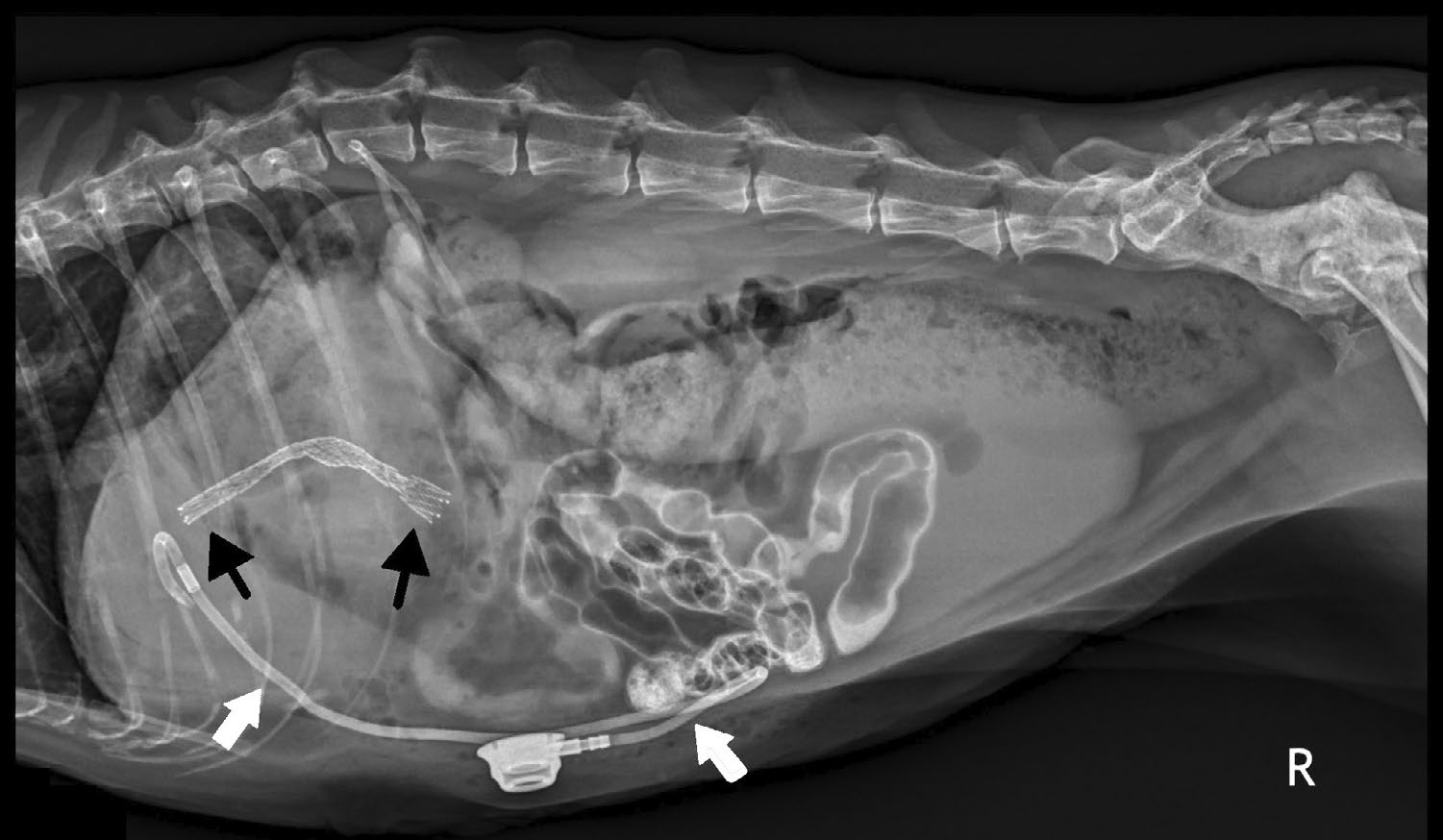
↑ 术后右侧腹部X光片。适当放置的胆道引流管(白色箭头)和支架(黑色箭头)。胆管造影后胃肠道内有持续的造影,显示胆道系统通畅。
腹部超声显示不对称胆道减压,持续右侧肝内胆道扩张(下图A)和左肝内胆道扩张消退(下图B)。观察到支架从十二指肠腔延伸穿过胆总管并进入胆道内的左外侧肝叶(下图C)。观察到大量回声性腹腔积液。液体分析符合轻度混合炎症,未见细菌,需氧和厌氧培养呈阴性。
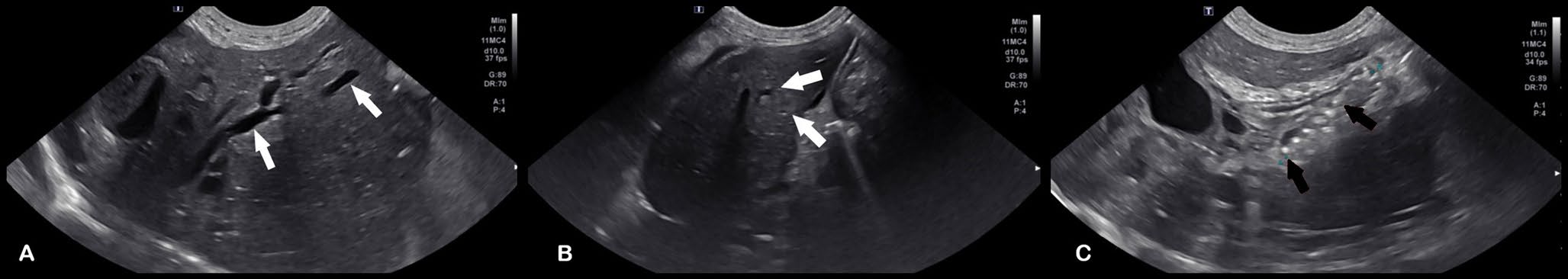
↑(A)右肝,肝内导管持续扩张(白色箭头)。(B)左肝内导管扩张消退(白色箭头)。(C)支架穿过胆总管(黑色箭头)。
术后3天,出院并过渡到肠内药物,包括阿莫西林/克拉维酸 (13.5 mg/kg PO q12h)、恩诺沙星 (4.9 mg/kg PO q24h)、昂丹司琼 (0.4 mg/kg PO q12h)、熊去氧胆酸(13.5 mg/kg PO q24h)和赛庚啶(0.4 mg/kg PO q12h)。
术后15天,出现厌食和反流。腹部超声显示胆道支架位置正常,右肝内导管持续扩张,左肝内导管扩张消退,腹膜积液轻度。胃胀气和低氯血症代谢性碱中毒的存在提示肠梗阻,但没有机械性阻塞的证据。住院接受静脉输液、补钾、氨苄西林/舒巴坦、恩诺沙星、多西环素、马罗吡坦、丁丙诺啡、加巴喷丁、泮托拉唑、昂丹司琼、 甲氧氯普胺、西沙必利和硫胺素。反流持续存在,超声显示进行性胃胀和腹腔积液,怀疑功能性肠梗阻或胆道肿瘤导致十二指肠近端流出道阻塞。没有看到胆道支架阻塞十二指肠腔。
术后19天,出现难治性低血压,被安乐死,没有进行尸检。
| 病例2 | |
 | 品种:短毛猫 |
| 年龄:8岁 | |
| 性别:雄 | |
| 是否绝育:是 | |
| 诊断:肝外胆道梗阻 | |
05 主诉及病史
进一步评估继发于胆管腺癌的胆道梗阻。
之前接受过腹部超声和剖腹探查术,发现胆道梗阻伴胆囊、肝管和胆囊管明显扩张,胆总管内肿块导致完全管腔阻塞。还患有胰腺炎和腹膜炎。进行了常规胆囊十二指肠造口术。肿块符合胆管腺癌。
既往治疗包括静脉输液、氨苄西林、恩诺沙星、昂丹司琼、马洛匹坦、法莫替丁、地那马林以及维生素B12和K1。
虽然在造口术后有所好转,高胆红素血症消退,但胆道梗阻在16天后复发。因持续严重的高胆红素血症、肝酶活性升高以及贫血、网织红细胞增多、单核细胞增多和血浆纤维蛋白原浓度升高而被送往医院。
06 治疗
体重3.95公斤。考虑手术干预以进行胆道支架置入术。术前给予维生素K1(0.6 mg/kg SC)和DDAVP(1.1 mg/kg SC)。
在腹部探查时,发现肿瘤阻塞了胆囊管,导致胆囊十二指肠造口术失败。如病例1所述,使用Rendezvous技术,并进行了一些修改。
胆道通路是通过左外侧肝叶扩张的肝内胆管完成的。顺行胆管造影证实梗阻(下图A)。
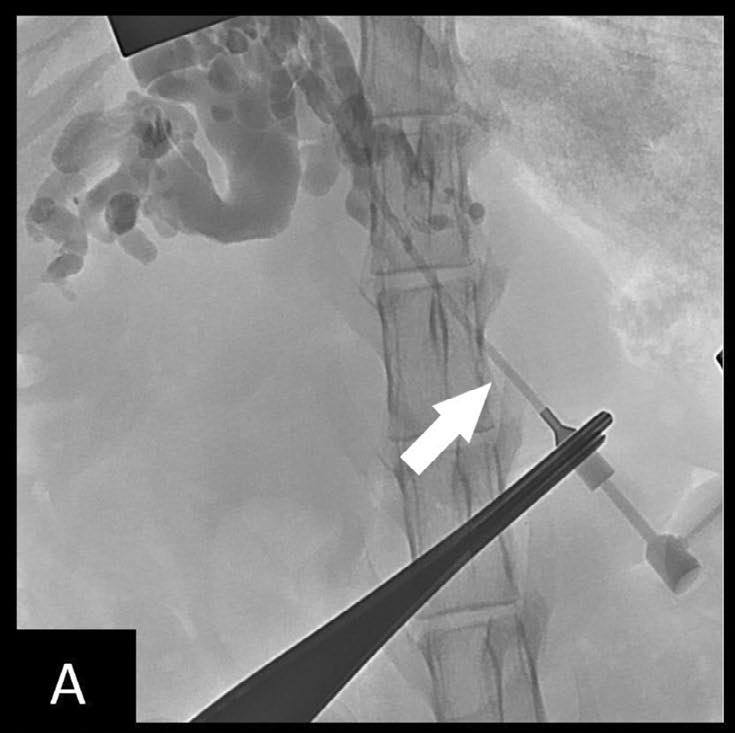
↑(A)透视显示导管(白色箭头)在肝内导管内,并成功进行了胆管造影。
如病例1所述,使用导丝和微穿刺系统,但由于胆脂肠造口术,导丝穿过胆囊管,进入胆囊,然后进入十二指肠(下图B)。
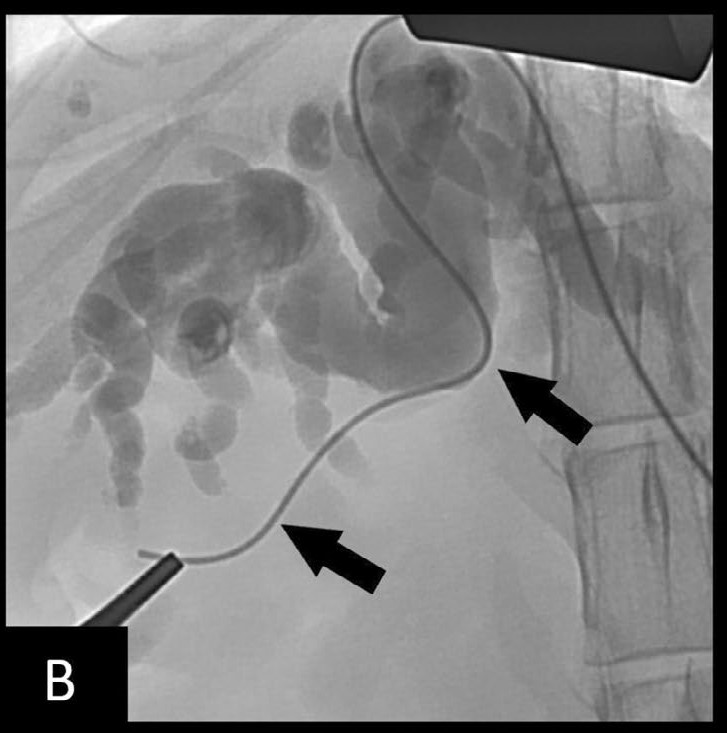
↑(B)亲水导丝(黑色箭头)穿过胆总管并进入十二指肠。
没有逆行支架放置,而是从左肝内胆管通路顺行放置胆道支架(4×60 mm),穿过胆囊管,离开胆囊内的胆囊十二指肠造口部位(下图C),与十二指肠相通。
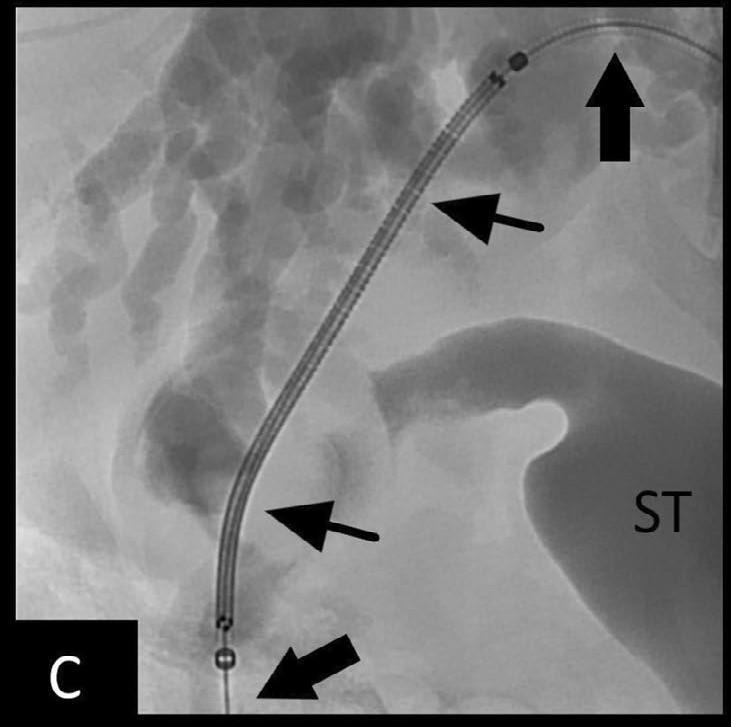
↑(C)胆道支架输送系统(黑色箭头)通过导线。在支架放置后,注意到胃的造影剂填充(ST)。
支架置入术后胆管造影证实胆道通畅(下图D)。再次将锁环导管推进到导丝上并放入左胆管,并将其留在原位,连接到皮下通路端口以进行潜在的化疗。总手术时间为111分钟。胆汁培养结果为粪肠球菌阳性。
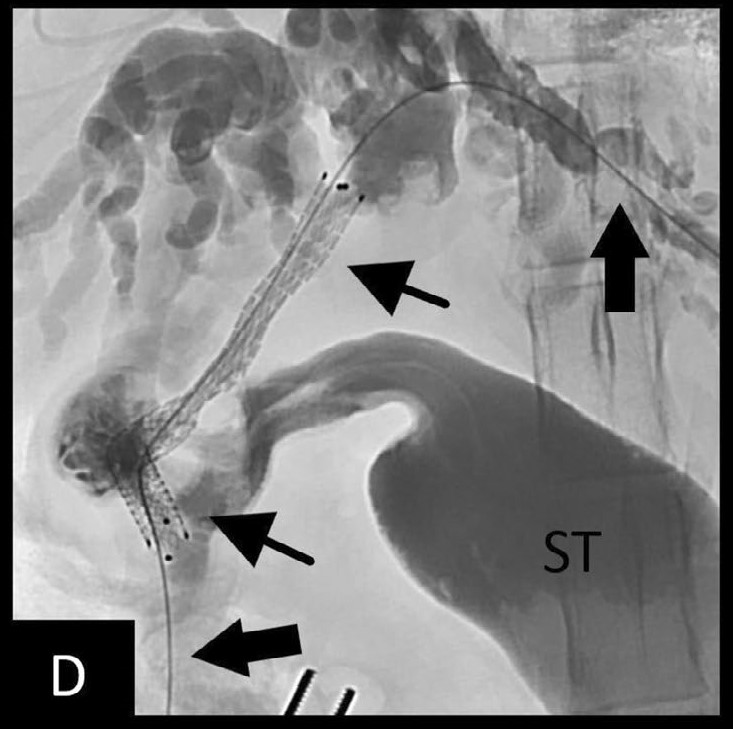
↑(D)胆管造影显示已部署的胆道支架通畅(黑色箭头)。
07 预后
接受了静脉输液,补充氯化钾、甲氧氯普胺(2 mg/kg/天 IV)、马罗吡坦(1 mg/kg IV q24h)、昂丹司琼(0.9 mg/kg IV q12h)、氨苄西林/舒巴坦(30 mg/kg IV q8h)、恩诺沙星(5 mg/kg IV q24h)和美沙酮(0.2 mg/kg IV q6h)。
术后观察到高胆红素血症的改善和肝酶活性的增加。术后X光片显示支架和胆道引流管放置得当(下图)。当管子进入体壁时,可以看到管子有部分扭结,但没有临床后果。
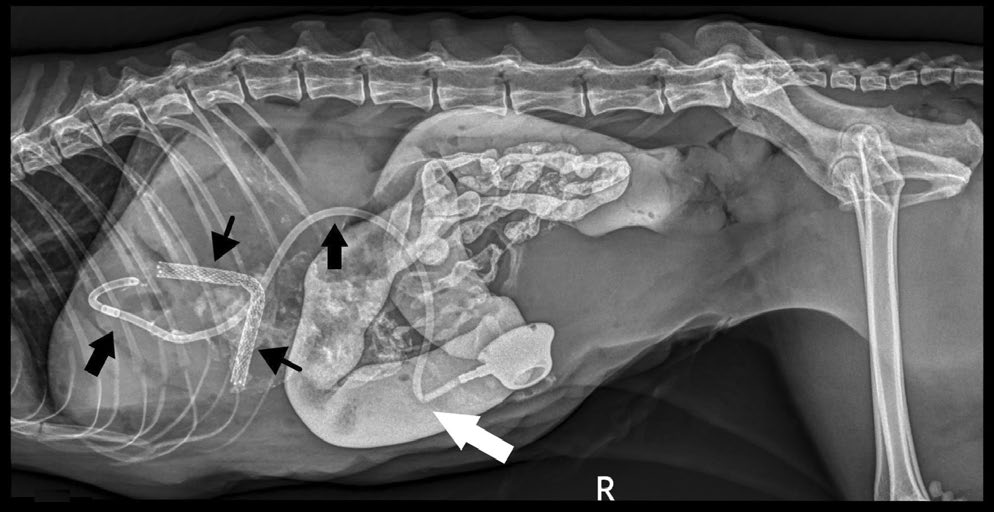
↑ 适当放置的胆道引流导管(粗黑色箭头)和支架(细黑色箭头)。胆道引流导管中有一个扭结(白色箭头)。胃肠道内存在持续的造影剂。
超声显示肝内胆管不对称减压,右胆道阻塞持续,左侧减压(下图)。还注意到腹腔积液。
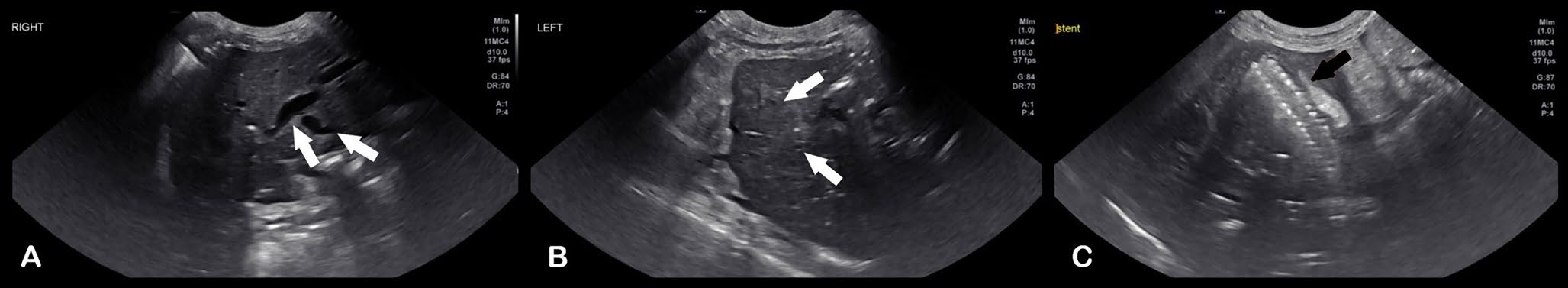
↑(A)右肝肝内导管持续扩张(白色箭头)。(B)左肝肝内导管扩张消退(白色箭头)。(C)支架穿过胆囊管(黑色箭头)。
术后1天出院,继续在转诊兽医处住院,并根据培养结果过渡到肠内多西环素。
术后3天,肝酶活性和血清胆红素浓度有所改善。
术后3周,血清胆红素和肝酶活性正常。CT扫描显示肺转移,并开始PO化疗。
术后63天,血清总胆红素浓度轻微升高,情况良好,没有左侧胆道扩张的证据。在此之后,患者失访。
08 讨论
肝外胆管梗阻(Extrahepatic biliary duct obstruction,EHBDO)与多种基础疾病相关,并在数周内导致严重肝胆损伤。
一项针对41例犬和4例猫EHBDO病例的回顾性研究发现,最常见的原因是胰腺炎(42%),其次是腔外和腔内肿瘤(24.3%)、胆管炎(17.8%)和胆石症(8.8%)。仅评估猫病例时,肿瘤是最常见的病因(75%)。
EHBDO的传统治疗包括剖腹胆管改道或通过十二指肠切开术在十二指肠大乳头放置胆道支架。
据报道,胆道改道技术在狗和猫中的围手术期死亡率分别为28%-67%和41%-57%。胆道支架开放手术置入的围手术期死亡率分别为狗30.7%和猫21.7%-28%。
在过去十年中,使用介入放射学和内镜检查已被证明可以降低围手术期并发症和死亡率。内镜逆行胰胆管造影(ERCP)利用内镜和透视对胆总管和胰管进行成像。该技术已在44只狗和猫中报道,成功率为40%-67%。
在一项纳入7项研究和2只临床犬的研究中,该疗法已与减压胆道支架置入术(ERC-BS)或括约肌切开术相结合。最近一份关于14只狗和3只猫的ERCP报告显示,14/17(82%)狗和1/3(33%)猫成功减压。主要限制因素是需要胆总管插管,这对于十二指肠大乳头的阻塞性肿瘤患者尤其具有挑战性。
ERC-BS的替代方法是Rendezvous技术,通过穿刺使导丝进入到肝内胆管中,将导丝沿着十二指肠大乳头推进到十二指肠,从而进入胆道系统。一旦导丝进入十二指肠,就可以使用胃十二指肠镜和抓握器械将其取出并通过口腔拉出。
如果经皮进行,这在人类中最常见,则称为经皮经肝Rendezvous技术(PTE-RV)。一篇报道描述了PTE-RV治疗继发于感染性胆囊炎和狗矿化碎片的EHBDO。这只狗通过支架置入和基于培养结果的抗生素治疗完全康复。
在本病例中,PTE-RV的改良版本用于治疗两只手术选择有限的猫的弥漫性恶性胆道梗阻。结果表明,如果超声中可以看到肝内胆管,则该技术可用于猫以减压胆道系统。该手术提供了更传统的外科干预的替代方案,例如胆囊造口术(CCE)或通过肠切开术进行的传统手术辅助胆道支架置入术,特别是在恶性梗阻可能阻塞整个胆道的情况下。
与传统CCE相比,PTE-RV在技术上更快且侵入性更小。在病例1中,进行了CCE但失败了,而在病例2中,胆囊管被阻塞,使得CCE不可行。由于肿瘤定位和十二指肠大乳头消失,以及患者体型较小,传统的ERCP无法进行逆行支架置入术。
总之,改良的PTE-RV手术在2只患有恶性EHBDO的猫中在技术上是成功的。该技术提供了传统手术治疗的替代方案,特别是在无法进行ERC-BS时。需要更多的研究来评估长期结局并评估胆道梗阻良性原因的效用。
文献来源:Doherty R, Berent AC, Weisse C. Use of a Modified Transhepatic Rendezvous Technique for Stenting of Malignant Biliary Obstruction in 2 Cats. J Vet Intern Med. 2025 Jul-Aug;39(4):e70178.