
| 一般情况 | |
 | 品种:布偶猫 |
| 年龄:10岁 | |
| 性别:雄 | |
| 是否绝育:是 | |
| 诊断:慢性肾病 | |
01 主诉及病史
慢性肾病(CKD)复查。
2023年8月,因厌食、恶心、呕吐、嗜睡和体重进行性减轻就诊。体重6.3公斤,体况评分5/9,黏膜苍白。血肌酐(SCr)为280 μmol/L [71-212],尿素氮(BUN)为16.8 mmol/L [5.7-12.9]。诊断为IRIS CKD III期。经过基本的支持治疗后,临床症状消退,体重稳定在5.7公斤。于11月中旬出院进行家庭管理。
02 检查
2024年6月下旬复诊,体重4.6公斤,体况评分1/9,黏膜苍白。影像学检查发现左肾肿大(4.55 cm)、右肾萎缩(3.25 cm)、肾皮质增厚、高回声和皮质髓分化丧失(下图)。
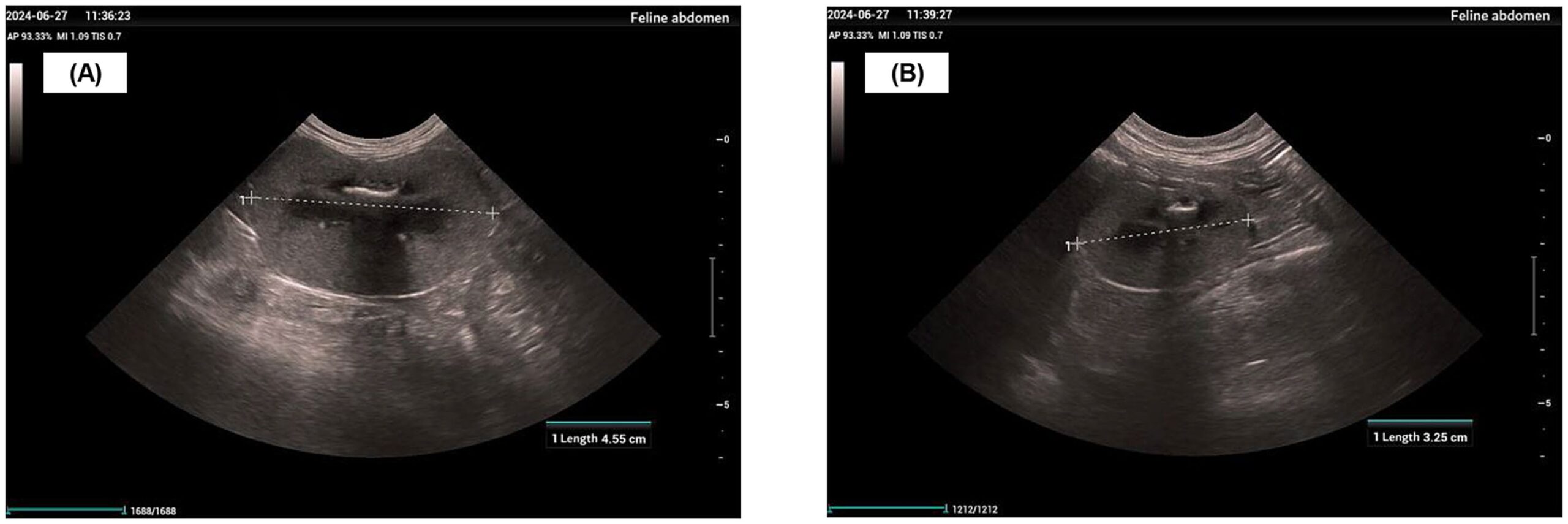
↑ 肾脏超声图像。(A)左肾。(B)右肾。
血生化显示SCr为799 μmol/L,BUN>46.4 mmol/L,磷>5.20 mmol/L [1.00–2.42]。诊断为IRIS CKD IV期。
住院治疗计划包括乳酸林格氏液(q24h 200 mL SC)、马罗吡坦(q24h 1.0 mg/kg SC)、替米沙坦(q24h 1.0 mg/kg PO)和达依泊汀α(每7天 1.0 μg/kg SC),此外还有肾脏处方饮食和营养保健品。
尽管使用了IRIS指南推荐的疗法,但SCr、BUN和磷水平仍持续高于正常值。患者的状态较差,在征得主人同意的情况下,开始间充质干细胞治疗,以减少慢性肾脏病对肾脏的进一步损害,缓解临床症状,提高患者的生活质量。
03 治疗
脂肪组织是从一只9个月大的健康布偶猫(供体猫)身上无菌获得的(下图A),该猫血液学参数正常,传染病筛查阴性。样品用磷酸盐缓冲液冲洗3次,然后保存到含有磷酸盐缓冲液和1%青霉素-链霉素的离心管中。
将脂肪组织剪碎消化后,过滤重悬获得间充质干细胞。对间充质干细胞的显微镜分析显示,具有典型的纺锤形纤维细胞样外观(下图B-D)。通过流式细胞术确认了猫脂肪来源细胞的特征,包括CD29、CD44、CD90、CD105阳性,CD34阴性(下图E-I)。当在分化培养基中培养时,间充质干细胞表现出三系分化潜力,可分化为脂肪细胞,成骨细胞和软骨细胞(下图J-L)。
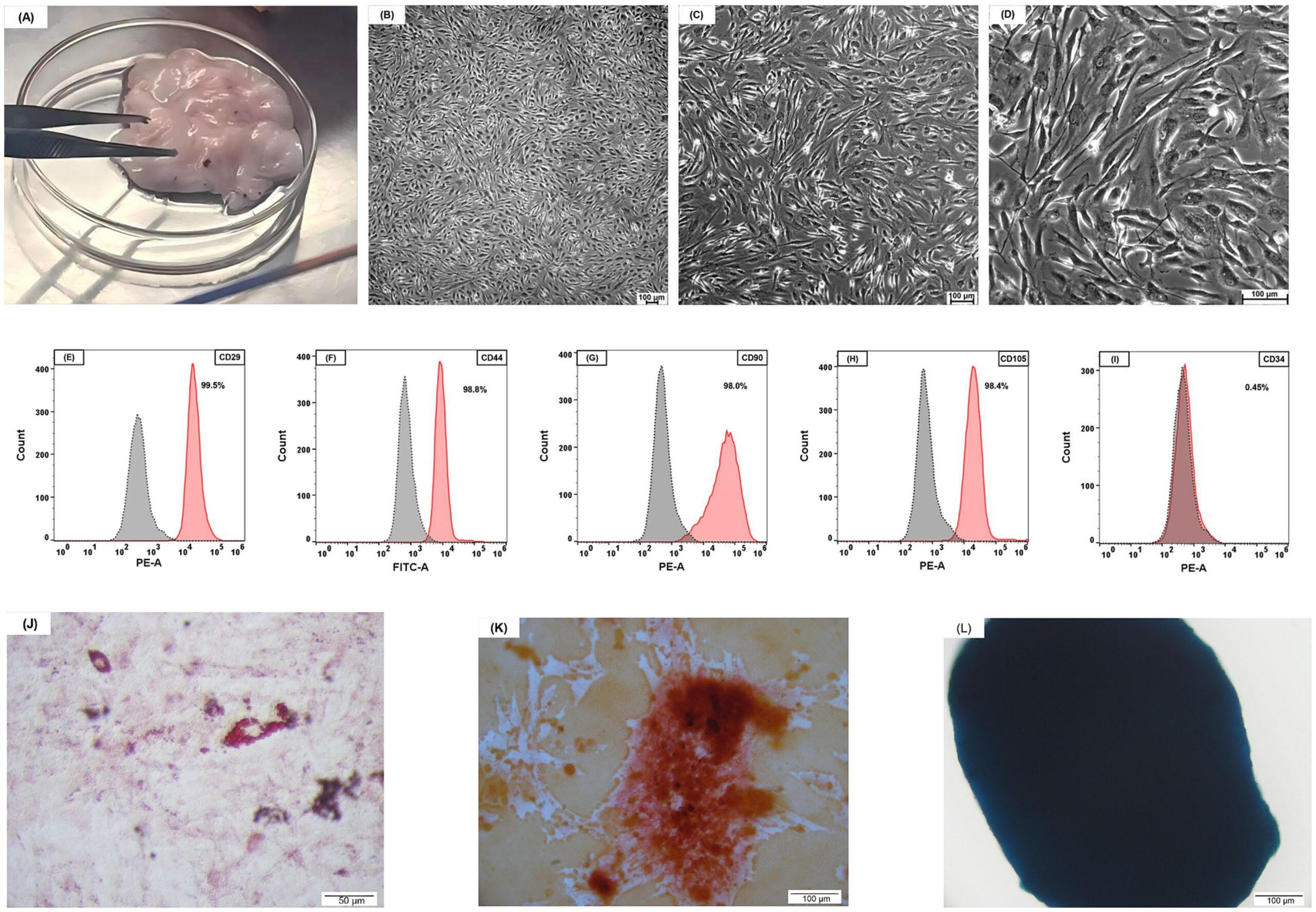
↑ 猫脂肪组织和脂肪源性间充质干细胞的表征。(A)猫脂肪组织。(B)50倍放大倍率;(C)100倍放大倍率;(D)200倍放大倍率,脂肪源性间充质干细胞表现出纺锤形形态。(E-I)脂肪源性间充质干细胞高表达CD29、CD44、CD90和CD105,但不表达CD34。(J)成脂分化,油红O染色。(K)成骨分化,茜素红染色。(L)软骨分化,阿尔新蓝染色。
将冷冻保存的脂肪源性间充质干细胞(AD-MSC)解冻并培养,洗涤后将细胞重悬于1 mL细胞冷藏保存预混材料中,该材料不含二甲基亚砜和动物源性成分。立即将细胞悬液转移到无菌小瓶中,并在2-8°C下避光储存,且在24小时内输注。
输注前,抽取细胞悬液并将其添加到装有50 mL盐水的输液瓶中。AD-MSC最终剂量为8.8×10^6个细胞/50 mL(相当于2×10^6个细胞/kg)通过静脉导管在60分钟内缓慢输注。
为了降低输液反应的风险,预先给予地塞米松(0.5 mg/kg)。在整个输注过程中和输注后30分钟内持续监测生命体征,观察时间延长至24小时。
04 预后
治疗期间或治疗后未观察到发热或呕吐等不良反应。
第一次干细胞注射1周后,SCr为731 μmol/L。
第二次干细胞注射1周后,SCr降至636 μmol/L。第三次干细胞注射1周后,SCr降至495 μmol/L。
第三次干细胞注射3周后,SCr降至204 μmol / L,属于CKD II期的参考范围(下图A)。BUN降至24 mmol/L,磷降至2.73 mmol/L(下图BC)。在整个治疗期间,患者的精神状态和食欲有所改善。体重恢复至5公斤,体况评分改善至3/9,黏膜恢复为粉红色。在随后的随访期间,体重和体况评分均有所改善,肌酐、尿素氮和磷水平下降,肾性贫血改善。
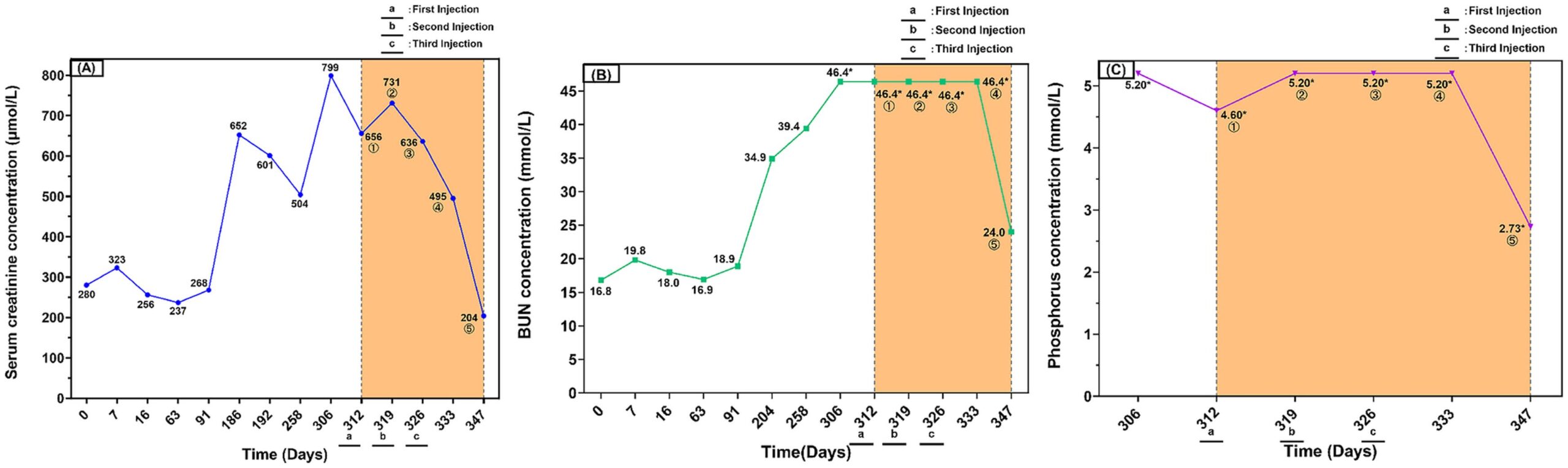
↑(A)随时间变化的SCr浓度。(B)随时间变化的BUN。(C)随时间变化的血清磷浓度。黄色阴影区域表示AD-MSC处理时期。图上带圆圈的数字①-⑤表示以下时间点:①第一次注射前(基线);②第二次注射前;③第三次注射前;④第三次注射后1周;⑤第三次注射后3周。*表示达到仪器检测范围上限。第0天定义为2023年8月首次住院后开始治疗的那天,作为临床时间表的基线。a、b和c分别表示第一次、第二次和第三次间充质干细胞输注的时间点。
05 讨论
猫慢性肾病(Chronic kidney disease,CKD)是一种以肾脏结构或功能异常持续超过3个月为特征的代谢性疾病,是猫医学中最常见的疾病之一。
流行病学研究表明,CKD在猫中的发病率高于犬,尤其在老年猫中更为常见,尽管任何年龄的猫都可能发病。
CKD的主要组织学特征包括肾小球硬化、肾小管间质炎症、萎缩和纤维化。目前,猫CKD尚无广泛认可的治愈药物,治疗主要集中在支持性和对症治疗上,旨在改善受影响猫的生活质量和延缓疾病进展。
本病例中,一只10岁的布偶猫因厌食、恶心、呕吐、倦怠和进行性体重减轻而就诊,被诊断为国际肾脏疾病协会(IRIS)CKD III期。经过基础支持治疗后,症状缓解,但3个月后病情恶化,达到IRIS CKD IV期。尽管按照IRIS指南进行了4个月的支持治疗,但临床症状和实验室指标均无显著改善,猫仍处于恶病质状态。
随后,采用了异体脂肪源性间充质干细胞(AD-MSC)治疗,每周静脉注射一次,连续3周。治疗后,血清肌酐、尿素氮和磷水平均有所改善,精神状态和食欲也有所提高,肾功能从IV期改善至II期。
本病例中,AD-MSC治疗显示出良好的安全性,未观察到发热或呕吐等不良反应。治疗后,猫的肾功能指标显著改善,精神状态和食欲也有所提高。这表明AD-MSC可能通过其分泌的多种生物活性因子(如血管内皮生长因子、成纤维细胞生长因子、肝细胞生长因子等)发挥肾脏保护作用。
然而,本病例也存在一些局限性。这是一项单病例研究,样本量有限,无法充分证实AD-MSC治疗的疗效。虽然研究探讨了AD-MSC的旁分泌机制,但未深入研究这些机制在本病例中的具体分子途径。此外,本研究为开放性设计,兽医和主人均知晓进行了干细胞治疗,可能存在安慰剂效应,影响对主观结果(如食欲、精神状态和行为)的评估。
总之,本病例报告表明,异体AD-MSC治疗可能对猫晚期CKD具有潜在的治疗效果。未来的研究应增加样本量,采用对照试验设计,并进行长期随访,以明确AD-MSC治疗在慢性肾病中的长期疗效和潜在不良反应。此外,未来研究还应关注AD-MSC的预处理技术,如缺氧预处理和褪黑素预处理,以提高AD-MSC的治疗效果。AD-MSC治疗在CKD管理中具有阶段依赖性,早期干预可获得最佳效果,但在晚期CKD中效果可能有限,因此需要发现预测性生物标志物,以便早期识别CKD。
文献来源:Song Y, Liu Y, Yu Y, Wang Y, Mu Y, Wang S, Han W, Zhang H, Zhang W. Case Report: Allogeneic adipose-derived mesenchymal stem cells for severe feline chronic kidney disease. Front Vet Sci. 2025 Jul 23;12:1632324.